Наука, която можеш да почувстваш
Хранителни добавки базирани на десетилетия изследвания в областта на метилирането—биохимичният процес, който управлява твоята енергия, настроение и дълголетие.
Метилиране

Знаеш ли, че...
Метилирането се случва 300 милиарда пъти на ден в твоето тяло? Tези реакции са критични за оцеляването и процъфтяването на клетките ти.
Над 50% от населението по света има генетична вариация в MTHFR гена, което означава, че техните тела не могат ефективно да преобразуват стандартната фолиева киселина в използваема метилфолат форма.

Какво е метилиране?
Метилирането е биохимичен процес, при който към молекула се добавя метилова група (CH3 - един въглерод и три водородни атома). Този процес представлява може би най-важният биохимичен процес за дълголетието и оптималното здраве.
Как метилирането участва в:
Производството на енергия
Метилирането е в основата на енергийното производство в митохондриите - "електроцентралите" на клетките. Без оптимално метилиране:
ATP производството спада - ATP е енергийната валута на клетката. Метилирането поддържа коензим Q10 и креатин синтеза
Митохондриалната функция се нарушава - Метилирането на митохондриалната ДНК е критично за експресията на енергийни гени
NADH/NAD+ балансът се измства - Това води до метаболитен стрес и ускорено стареене
Клинични доказателства:
Проучване в Molecular Genetics and Metabolism (2015) показва, че хора с MTHFR мутации имат 25-40% по-ниска митохондриална активност в сравнение с контролна група.
Източници:
Loehrer, F.M., et al. (2001). "Impaired DNA methylation in the mitochondria" Circulation 104:2569-2575
Suormala, T., et al. (2004). "Mitochondrial metabolism and function in MTHFR deficiency" Molecular Genetics and Metabolism 83:208-213
Детоксикацията
Метилирането е критично за трите фази на детоксикация в тялото:
Фаза I - Активация:
Токсините се "маркират" за елиминация чрез окисляване.
Фаза II - Конюгация (тук метилирането е ключово):
Глутатион конюгация - Метилирането произвежда глутатион, най-мощният антиоксидант
Сулфация - Изисква SAMe за метаболизма на серен и цистеин
Ацетилация - За детокс на ароматни амини
Фаза III - Транспорт:
Конюгираните токсини се изхвърлят през урината и жлъчката.
Какво се детоксифицира чрез метилиране:
✓ Тежки метали (олово, живак, арсен, кадмий)
✓ Пестициди и хербициди
✓ Пластификатори (BPA, фталати)
✓ Лекарствени метаболити
✓ Алкохол и ацеталдехид
✓ Естрогенови метаболити
✓ Пикочна киселина
✓ Хистамин
Исторически случай:
Проучване в Environmental Health Perspectives (2008) показва, че хора с MTHFR C677T мутация имат 2.5 пъти по-висока концентрация на тежки метали в кръвта в сравнение с wild-type генотип.
Източници:
Chen, W., et al. (2008). "MTHFR polymorphisms and heavy metal accumulation" Environmental Health Perspectives 116:447-453
Lu, S.C. (2009). "Regulation of glutathione synthesis" Molecular Aspects of Medicine 30:42-59
James, S.J., et al. (2004). "Metabolic biomarkers of oxidative stress" American Journal of Clinical Nutrition 80:1611-1617
Производството на невротрансмитери
Метилирането контролира синтеза на всички основни "химикали на щастието" в мозъка:
Серотонин (5-HT) - "Молекулата на щастието":
Метилфолатът е кофактор за триптофан хидроксилаза (THP)
THP преобразува триптофан → 5-HTP → серотонин
Ниското метилиране → депресия, тревожност, нарушен сън
Допамин - "Молекулата на мотивацията":
SAMe метилира тирозин → L-DOPA → допамин
Регулира мотивация, награда, движение
Дефицит → прокрастинация, ADHD, Паркинсон
Норадреналин/Адреналин - "Молекулите на фокуса":
Допамин бета-хидроксилаза изисква SAMe
Критични за будност, стресов отговор, кръвно налягане
Дефицит → мозъчна мъгла, умора, хипотония
Ацетилхолин - "Молекулата на паметта":
Фосфатидилхолин (от холин и SAMe) → ацетилхолин
Критичен за памет, учене, мускулен контрол
Мелатонин - "Молекулата на съня":
Серотонин → N-ацетилсеротонин → мелатонин
Изисква SAMe за N-ацетил трансфераза
Регулира циркадния ритъм
Клинично доказателство:
Meta-analysis в American Journal of Psychiatry (2012) показва, че L-метилфолат като адювант към антидепресанти увеличава ремисията 7.2 пъти при пациенти с депресия.
Източници:
Papakostas, G.I., et al. (2012). "L-methylfolate augmentation in major depression" American Journal of Psychiatry 169:1267-1274
Miller, A.L. (2008). "The methylation, neurotransmitter, and antioxidant connections" Alternative Medicine Review 13:216-226
Репарация на ДНК
Метилирането може да се нарече "ДНК техник". Всяка клетка в твоето тяло получава 10,000-100,000 ДНК увреждания на ден от:
Ултравиолетова радиация
Окисл олителен стрес
Репликационни грешки
Токсични експозиции
Как метилирането репарира ДНК:
Base Excision Repair (BER):
SAMe метилира DNA метил трансферази (DNMTs)
Премахват се увредени бази
Метилфолатът доставя нуклеотиди за замяна
Нуклеотиден Ексцизионен Репер (NER):
Метилирането активира репарационни ензими
Премахват се големи ДНК лезии
Хистонови Модификации:
SAMe метилира хистони → контролира достъпа до ДНК
Регулира кои гени са "включени" или "изключени"
Последици от лоша ДНК репарация:
Ускорено клетъчно стареене
Повишен риск от рак
Невродегенерация
Хронично възпаление
Проучване:
Nature Reviews Genetics (2007) публикува, че дефектното метилиране удвоява скоростта на ДНК мутации и е свързано с 50% от всички ракови заболявания.
Източници:
Esteller, M. (2007). "Cancer epigenomics: DNA methylation and cancer" Nature Reviews Genetics 8:286-298
Choi, S.W., et al. (2009). "Folate and DNA methylation" American Journal of Clinical Nutrition 89:1690S-1695S
Регулирането на хормони
Метилирането директно влияе на производството, активността и елиминацията на всички основни хормони:
Естроген метаболизъм:
SAMe метилира катехол-естрогени → безопасни метилирани форми
Лошо метилиране → натрупване на токсични 4-OH естрогени
Свързано с рак на гърда, миоми, ендометриоза
Тестостерон:
Метилирането регулира андроген рецепторна чувствителност
SAMe е критичен за креатин синтеза (мускулна маса)
Тиреоидни хормони:
Метилирането влияе на T4 → T3 конверсия
Лошо метилиране може да имитира хипотиреоидизъм
Кортизол:
COMT ензимът (зависим от SAMe) разгражда адреналин
Дефектно метилиране → хроничен стрес, "жица" чувство
Инсулин:
Метилирането влияе на инсулинова сигнализация
Епигенетични промени водят до диабет тип 2
Източници:
Zhu, B.T. (2002). "Catechol-O-Methyltransferase in estrogen metabolism" Endocrine Reviews 23:724-738
Jaenisch, R., et al. (2003). "Epigenetic regulation in metabolic diseases" Nature Reviews Genetics 4:638-649
Имунната система
Оптималното метилиране е критично за балансирана имунна функция:
Глутатион - "Майсторският Антиоксидант":
Произвежда се чрез трансулфурационния път (зависим от метилиране)
Рециклира други антиоксиданти (витамин C, E)
Детоксифицира патогени и свободни радикали
Дефицитът е свързан с всички автоимунни заболявания
NK (Natural Killer) клетки:
Метилирането регулира NK клетъчната активност
NK клетките елиминират ракови клетки и вируси
T-клетъчна функция:
DNA метилирането диференцира T-helper 1 vs T-helper 2 баланс
Дисбалансът води до автоимунитет или алергии
Цитокини:
Метилирането регулира възпалителни цитокини (TNF-α, IL-6, IL-1β)
Лошо метилиране → хронично възпаление
Автоимунни заболявания свързани с дефектно метилиране:
Ревматоиден артрит
Системен лупус еритематозус (SLE)
Множествена склероза
Целиакия
Тиреоидит на Хашимото
Източници:
Lu, S.C. (2013). "Glutathione synthesis and immune function" Biochimica et Biophysica Acta 1830:3143-3153
Jeffries, M.A., et al. (2011). "DNA methylation in autoimmunity" Clinical Immunology 140:242-251
Niculescu, M.D., et al. (2006). "Nutritional genomics and inflammatory diseases" Annual Review of Nutrition 26:131-155
Защо здравословното метилиране е критично важно?
50%+
от хората имат генетична вариация в MTHFR гена
73%
от възрастните имат субоптимални нива на фолат
68%
не получават достатъчно B12 от храната
40%
от хората над 50 години имат хомоцистеин >10 µmol/L
Когато метилирането не работи оптимално, последствията засягат цялото тяло
Неврологичното здраве
Връзката между мозъкът и метилирането е критична. Мозъкът е изключително зависим от метилиране поради:
Висока енергийна нужда (20% от телесната енергия за 2% от теглото)
Интензивна невротрансмитерна активност
Постоянна ДНК репарация в неврони
Миелинов синтез и поддръжка
Неврологични състояния свързани с дефектно метилиране:
Депресия:
30-40% от хората с депресия имат MTHFR мутации
Ниското метилиране води до намален серотонин, допамин, норадреналин
L-метилфолат увеличава ремисията 7.2 пъти като адювант към SSRI
Тревожност:
Gary Brecka: "Тревожността от MTHFR има три характеристики: присъства цял живот, без ясен тригер, и не реагира добре на стандартно лечение"
Дефектното метилиране води до дисбаланс на GABA и серотонин
ADHD:
Деца с MTHFR мутации имат 2-3 пъти по-висок риск от ADHD
Метилфолат суплементацията подобрява вниманието и поведението
Мозъчна мъгла:
"Brain fog" е класичен симптом на лошо метилиране
Причинено от ниски невротрансмитери + намалено ATP производство
Деменция и Алцхаймер:
Повишеният хомоцистеин увеличава риска от Алцхаймер с 40-50%
Мета-анализ показва, че B витамини забавят мозъчна атрофия с 30%
Периферна невропатия:
B12 и фолат дефицитът водят до деми елинизация
Причинява изтръпване, болка, загуба на баланс
Мигрена:
40% от хората с мигрена с аура имат MTHFR мутации
Високият хомоцистеин е триггер за съдови главоболия
Източници:
Papakostas, G.I., et al. (2012). "L-methylfolate in depression" American Journal of Psychiatry 169:1267-1274
Bottiglieri, T. (2005). "Homocysteine and neuropsychiatric disorders" Nutritional Neuroscience 8:291-297
Smith, A.D., et al. (2010). "Homocysteine-lowering and brain atrophy" PLoS ONE 5:e12244
Haan, M.N., et al. (2007). "Homocysteine, B vitamins, and Alzheimer disease" Neurology 69:917-924
Сърдечно-съдовата система
Метилирането е жизненоважната връзка за сърдечното здраве. Сърдечно-съдовите заболявания са причина #1 за смърт в света. Дефектното метилиране е основен, но пренебрегван рисков фактор.
Хомоцистеин - "Тихият убиец":
Хомоцистеинът е аминокиселина, която се натрупва когато метилирането е нарушено. Високите нива са също толкова опасни колкото пушенето или високият холестерол.
Оптимални нива: <7 µmol/L
Гранични нива: 7-10 µmol/L
Рискови нива: >10 µmol/L
Високо рискови: >15 µmol/L
Рискове при повишен хомоцистеин:
3x по-висок риск от инфаркт на миокарда
2.5x по-висок риск от инсулт
1.6x по-висок риск от венозна тромбоза
2x по-висок риск от периферна артериална болест
Механизми на увреждане:
Ендотелиална дисфункция - Хомоцистеинът увреждаобвивката на кръвоносните съдове
Оксидативен стрес - Генерира свободни радикали
Тромбоза - Повишава кръвната съсирваемост
Възпаление - Активира CRP, IL-6, TNF-α
Гладко-мускулна пролиферация - Задебелява артериалните стени
Хипертония (високо кръвно):
Хомоцистеинът намалява азотен оксид (NO) → съдово свиване
Хора с MTHFR мутации имат по-висок риск от хипертония
Атеросклероза:
Мета-анализ: Всяко 5 µmol/L увеличение на хомоцистеина = 20% повече атеросклеротична плака
Хомоцистеинът ускорява LDL окислението
Сърдечна недостатъчност:
Високият хомоцистеин е независим предиктор за сърдечна недостатъчност
Вероятност за хоспитализация нараства с 30% на всеки 5 µmol/L
Клинични проучвания:
HOPE-2 Trial (2006, N Engl J Med):
5522 пациенти с съдови заболявания
Фолат + B12 намалят инсултите с 25%
Norwegian Vitamin Trial (NORVIT) (2006):
Смесени резултати, но подгрупов анализ показва полза при хора без B-fortified храни
Meta-analysis на 19 проучвания (2010, Arch Intern Med):
Фолат суплементация намалява риска от инсулт с 18%
Източници:
Wald, D.S., et al. (2002). "Homocysteine and cardiovascular disease: evidence on causality from a meta-analysis" BMJ 325:1202
Homocysteine Studies Collaboration (2002). "Homocysteine and ischemic heart disease" JAMA 288:2015-2022
Clarke, R., et al. (2010). "Effects of lowering homocysteine on cardiovascular disease" Archives of Internal Medicine 170:1622-1631
Lonn, E., et al. (2006). "Homocysteine lowering with folic acid in vascular disease" New England Journal of Medicine 354:1567-1577
Енергията и метаболизма
Метилирането e като енергиен мост. Усещането за хронична умора е един от най-честите симптоми при дефектно метилиране.
Митохондриална дисфункция:
Метилирането регулира митохондриалната ДНК
Дефицитът води до намалено ATP производство
Резултат: Постоянна умора, мускулна слабост
Метаболитни пътища:
Креатинов синтез:
SAMe отдава метилови групи за креатин производство
Креатинът зарежда ATP в мускулите
Дефицит → мускулна умора, намалена сила
Коензим Q10:
Метилирането влияе на CoQ10 производството
CoQ10 е критичен за електронно-транспортната верига
Ниското CoQ10 → умора, мускулни болки
Карнитин синтез:
SAMe е необходим за L-карнитин производство
Карнитинът транспортира мастни киселини в митохондриите за горене
Дефицит → неефективно мастно изгаряне, умора
Тироидна функция:
Метилирането влияе на T4 → T3 конверсия
Субоптимално метилиране може да имитира хипотиреоидизъм
Симптоми: умора, нискаискова мъгла, запек
Кръвна захар и инсулин:
Епигенетични промени от лошо метилиране водят до инсулинова резистентност
Метилирането влияе на GLUT4 (глюкозен транспортер) експресия
Адренална функция:
SAMe е необходим за синтез на адреналин и норадреналин
"Адренална умора" често е всъщност метилационна дисфункция
Симптоми: умора сутрин, енергиен срив следобед
Източници:
Chango, A., et al. (2000). "Impaired methionine synthase and altered folate metabolism" American Journal of Clinical Nutrition 72:806-812
Obeid, R., et al. (2007). "Vitamin B12 and folate in cellular metabolism" European Journal of Clinical Investigation 37:748-754
Selhub, J. (2002). "Folate, vitamin B12 and cognitive decline" Nutrition Reviews 60:S38-S50
Репродуктивното здраве
Метилирането играе критична роля във всички аспекти на репродуктивното здраве—от зачеване до раждане.
Женски фертилитет:
Яйчно качество:
Метилирането влияе на митохондриалната функция в яйчните клетки
Жени с MTHFR мутации имат по-ниска овариална резерва (AMH)
Овулация:
Дефектното метилиране е свързано с PCOS (поликистозни яйчници)
Инозитол + метилфолат подобряват овулацията при PCOS
Имплантация:
Оптималното метилиране е критично за ендометриална рецептивност
Високият хомоцистеин намалява имплантацията с 30-50%
Бременност:
Дефекти на невралната тръба (NTDs):
Фолат дефицитът увеличава риска от спина бифида и анен цефалия
800 mcg фолиева киселина (или 400 mcg L-метилфолат) превентира 70% от NTDs
Жени с MTHFR мутации се нуждаят от по-високи дози
Спонтанен аборт:
Повишеният хомоцистеин увеличава риска от мизкерей с 2-3 пъти
Хиперкоагулабилност от хомоцистеин води до плацентарни тромбози
Прееклампсия:
Жени с MTHFR TT генотип имат 1.4x риск от прееклампсия
Високият хомоцистеин увреждаплацентарните съдове
Преждевременно раждане:
Лошото метилиране е свързано с повишен риск от преждевременно раждане
Възпалителни цитокини от дефектно метилиране тригъри раждането
Intrauterine Growth Restriction (IUGR):
Високият хомоцистеин намалява плацентарната перфузия
Плодът получава по-малко хранителни вещества
Мъжки фертилитет:
Сперматогенеза:
Метилирането регулира генната експресия във формирането на сперматозоиди
MTHFR мутации са свързани с олигоспермия (нисък брой сперматозоиди)
Качество на сперма:
Хомоцистеин >15 µmol/L намалява подвижността на сперматозоидите с 40%
ДНК фрагментацията в сперматозоидите се удвоява при лошо метилиране
Фолат и цинк подобряват морфологията на сперматозоидите
Клинично проучване: Проучване в Fertility & Sterility (2002) показва, че комбинацията от фолат (5mg) + цинк (66mg) увеличава броя на сперматозоидите с 74% при субфертилни мъже.
Източници:
Wong, W.Y., et al. (2002). "Effects of folic acid and zinc on male fertility" Fertility & Sterility 77:491-498
Ebisch, I.M., et al. (2007). "Homocysteine, folate and sperm quality" Molecular Human Reproduction 13:89-94
Nelen, W.L., et al. (2000). "Hyperhomocysteinemia and recurrent miscarriage" Fertility & Sterility 74:1196-1199
Ray, J.G., et al. (2001). "MTHFR and pregnancy complications" QJM 94:87-98
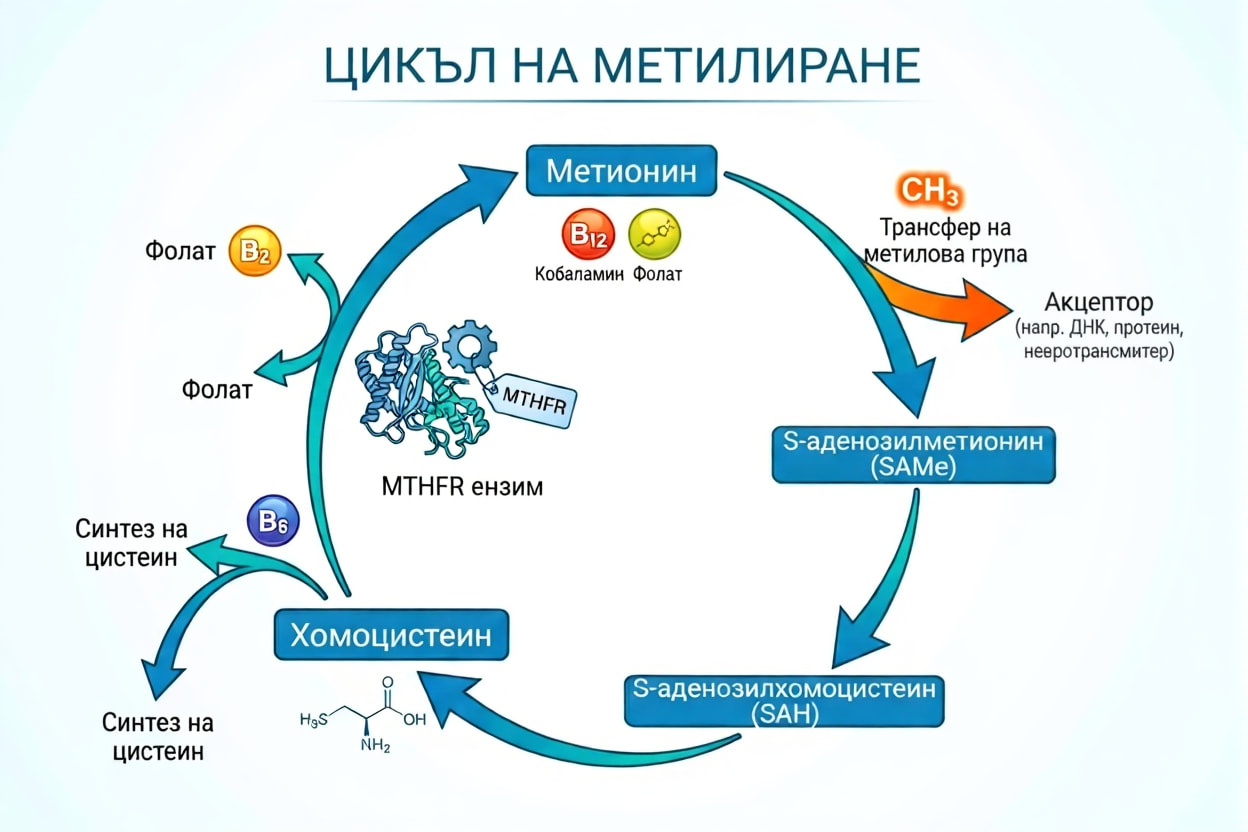
Критични кофактори за здравословен метилов цикъл:
Задължителни:
L-5-Метилфолат (активна форма на фолат)
Метилкобаламин (B12)
Пиридоксал-5-фосфат (B6)
Рибофлавин-5-фосфат (B2) - стабилизира MTHFR ензима
TMG (Бетаин) - алтернативен път
Поддържащи:
Магнезий - кофактор за 300+ ензима включително MAT
Цинк - кофактор за MTR и метаболизъм на фолата
Холин - предшественик на TMG
Стъпки на метиловия цикъл
Стъпка 1: Хомоцистеин → Метионин
Два пътя за рециклиране:
Път A (Фолатен път - 50% от рециклирането):
Хомоцистеин + 5-MTHF (метилфолат) + B12
↓ (чрез MTR ензим)
МетионинПът B (Бетаинов път - 50% от рециклирането):
Хомоцистеин + TMG (бетаин)
↓ (чрез BHMT ензим)
Метионин + DMGСтъпка 2: Метионин → SAMe
Метионин + ATP
↓ (чрез MAT ензим)
SAMe (S-аденозилметионин)Стъпка 3: SAMe → SAH (след отдаване на метилова група)
SAMe → Метилирана молекула + SAH (S-аденозилхомоцистеин)
Стъпка 4: SAH → Хомоцистеин
SAH
↓ (чрез AHCY ензим)
Хомоцистеин + Аденозин
Цикълът се затваря—хомоцистеинът отново се преобразува в метионин.
Какво спира метиловия цикъл:
Генетични блокажи:
MTHFR C677T/A1298C - намалена конверсия на фолиева киселина → метилфолат
MTR/MTRR - нарушен B12 метаболизъм
CBS - прекалено бърза конверсия на хомоцистеин → цистеин (рядко)
COMT - бавна деградация на катехоламини
MAT - намалено SAMe производство
Хранителни дефицити:
Липса на B витамини (B9, B12, B6, B2)
Недостиг на магнезий или цинк
Ниски нива на холин
Стрес и лайфстайл:
Хроничен стрес изчерпва магнезий и B витамини
Алкохол блокира фолат метаболизма
Пушене окислява B12
Лоша чревна здрава намалява B12 абсорбция
Токсични натоварвания:
Тежки метали (живак, олово) блокират метилиращи ензими
Пестициди и хербициди
BPA и фталати
MTHFR — генът засягащ половината човечество
Methylenetetrahydrofolate Reductase (MTHFR) е ензимът който преобразува фолиевата киселина в активен метилфолат.
Ако имаш MTHFR вариация, тялото ти не може ефективно да преобразува фолиевата киселина от храната или стандартните добавки в използваема форма.
Решението е просто: Вземай директно L-5-Метилфолат—формата която тялото използва незабавно, без да има нужда от преобразуване.
Решението - Оптимизиране на метилирането
Добрата новина: Оптимизирането на метилирането не изисква сложни протоколи или скъпи интервенции. Научните изследвания показват, че правилната комбинация от активни B витамини може да нормализира метиловия цикъл .
Л-метилфолат
Защо L-Метилфолат, а не фолиева киселина?
Фолиевата киселина е синтетична форма която изисква 4-5 ензимни стъпки за да стане използваема. Ако имаш MTHFR вариация, тялото ти не може ефективно да направи тази конверсия. L-5-Метилфолат е активната форма - готова за незабавна употреба, без нужда от преобразуване.
Клинично доказани ползи:
Намалява хомоцистеина с 20-30% за 4-6 седмици
Подобрява производството на серотонин и допамин - 7.2x по-ефективен за депресия (спрямо плацебо)
Заобикаля MTHFR блокажа напълно
Дозировки които работят:
Поддържаща: 400-1000 mcg дневно
Оптимизираща: 2.5-5 mg дневно
Терапевтична (депресия, висок хомоцистеин): 7.5-10 mg дневно
Източници: - Papakostas, G.I., et al. (2012). "L-methylfolate for SSRI-resistant depression" American Journal of Psychiatry 169:1267-1274 - Wald, D.S., et al. (2010). "Effect of folic acid on homocysteine" BMJ 341:c6273
Активни Б витамини
Защо активните Б витамини са критични за метилирането?
Активните Б витамини работят заедно с метилфолата за да рециклират хомоцистеина обратно в метионин. Без достатъчен B12, хомоцистеинът се натрупва - дори ако вземаш метилфолат.
Метилкобаламин срещу Цианокобаламин: Цианокобаламинът (евтината форма в повечето добавки) изисква конверсия в тялото. Метилкобаламинът е активната форма - директно използваема.
Кой се нуждае от повече B12:
Вегетарианци/вегани (нямат животински източници)
Хора над 50 години (намалена стомашна киселина)
Тези с чревни проблеми
Хора приемащи metformin или PPI медикаменти
Физически активни хора и атлети
Cellova Advanced B-Complex+ съдържа 1000 mcg метилкобаламин плюс всички други активни B витамини, в една дневна капсула.
TMH (Бетаин)
TMG (Trimethylglycine) е донор на метилови групи ДИРЕКТНО на хомоцистеина, заобикаляйки MTHFR ензима напълно.
Има два пътя за понижаване на хомоцистеин:
Път 1: Метилфолат → даване на CH3 група → Хомоцистеин става Метионин
Път 2: TMG → даване на CH3 група ДИРЕКТНО → Хомоцистеин става Метионин
Защо двата пътя работят по-добре заедно:
Метилфолат сам: 15-20% намаление на хомоцистеин
TMG сам: 10-20% намаление
И двете заедно: 30-40% намаление
Ако единият път е бавен (MTHFR мутация), другият компенсира.
Оптимална дозировка:
1000-2000mg TMG дневно (в комбинация с метилфолат)
Източници:
Schwab, U., et al. (2002). "Betaine lowers homocysteine" Journal of Nutrition 132:1879-1883
Оптимален Протокол
За всеки (базова оптимизация):
L-Метилфолат: 1-2.5mg дневно
TMG: 1000-2000mg дневно
Метилкобаламин B12: 1000mcg дневно
При висок хомоцистеин/MTHFR/симптоми:
L-Метилфолат: 5-10mg дневно
TMG: 2000-3000mg дневно
Метилкобаламин B12: 1000mcg дневно
Очаквани резултати:
Повече енергия
По-добър фокус
Подобрено настроение
По-добър сън
Хомоцистеин нормализиран
Здраво сърце
ДНК подпомагане
Подобрен детокс
Нормализирана нервна система
Подобрен имунитет
По-висока устойчивост на стрес
По-добра памет
Основни вещества за оптимизация на метилирането
Отключи по-здрави тяло и ум.
4.9
Пълна подкрепа на метилацията и оптимизация на клетъчното здраве.

4.8
L-Methylfolate⁺
Биоактивна форма на фолат, която заобикаля генетичните блокажи и достига директно до клетките.

4.8
8 висококачествени витамина от група B, работещи в синергия за пълноценно клетъчно усвояване.

4.6
Поддържа здравословната метилация и осигурява баланс в ключовите клетъчни процеси.
Често задавани въпроси
Какво е метилиране и защо е важно?
Метилирането е биохимичен процес при който се добавя метилова група (CH3) към молекули в тялото. То се случва 300 милиарда пъти на ден и влияе на енергията, детоксикацията, производството на невротрансмитери, репарацията на ДНК и над 200 други критични процеси в тялото.
Как да разбера дали имам проблем с метилирането?
Класични симптоми включват: хронична умора, тревожност, депресия, мозъчна мъгла, нарушен сън, проблеми с фертилитета. Можеш да направиш:
Хомоцистеин тест (цел: <7 µmol/L)
MTHFR генетичен тест
Опитай метилирана суплементация за 4 седмици и проследи подобренията
Какво е MTHFR мутацията?
MTHFR е ензим който преобразува фолиева киселина в метилфолат. 44-60% от хората имат генетична вариация (C677T или A1298C) която намалява ензимната активност с 30-70%. Това означава че тялото не може ефективно да използва фолиевата киселина от храната или добавките.
Трябва ли да правя генетичен тест за MTHFR?
Не е задължително, но е полезно. Ако имаш симптоми или фамилна история на сърдечни заболявания, инсулт, депресия или проблеми с фертилитета - тестът може да бъде много информативен. Въпреки това, ако вече имаш симптоми, можеш директно да започнеш метилирана суплементация и да проследиш резултатите.
Трябва ли да имам MTHFR мутация за да взимам метилфолат?
Не. L-метилфолатът е по-ефективната, биодостъпна форма на фолат за всеки - дори без MTHFR мутация. Той се усвоява по-добре и работи по-ефективно от фолиевата киселина. Всеки който иска оптимално здраве може да се възползва.
Безопасно ли е да вземам високи дози L-метилфолат?
Да. L-метилфолатът е водноразтворим витамин и излишъкът се елиминира през урината. Дози до 15mg дневно са използвани безопасно в клинични проучвания. Редки странични ефекти могат да включват лека тревожност при "свръхметилатори" - в този случай намали дозата.
Какво е разликата между фолиева киселина и L-метилфолат?
Фолиевата киселина е синтетична форма която изисква 4-5 ензимни стъпки да стане използваема. L-метилфолатът е активната, биодостъпна форма - готова за незабавна употреба. При хора с MTHFR мутации, фолиевата киселина може дори да блокира фолатните рецептори.
Мога ли да получа метилфолат от храната?
Да, но в много по-малки количества. Естественият фолат се намира в тъмно-зелени листни зеленчуци, говежди черен дроб и леща. Но за терапевтични цели (особено при MTHFR мутация), суплементацията е необходима.
Защо TMG и метилфолат заедно?
TMG и метилфолатът работят чрез ДВА различни пътя за понижаване на хомоцистеин. Метилфолатът използва MTHFR пътя, TMG го заобикаля напълно. Заедно постигат 30-40% намаление на хомоцистеин, срещу 10-20% поотделно. Ако единият път е бавен, другият компенсира.
Мога ли да взимам метилфолат ако съм бременна?
Да - всъщност метилфолатът е препоръчителен по време на бременност, особено при жени с MTHFR мутации. Той намалява риска от neural tube defects по-ефективно от фолиевата киселина. Консултирай се с лекар за правилната дозировка.
Каква е вашата гаранция?
Предлагаме 60-дневна гаранция за връщане на пари.
Добавките, които Cellova Health произвежда не са просто тенденция или спекулативни—резултатите им са доказани от стотици научни и клинични проучвания. Тези хранителни вещества са препоръчвани от водещи лекари, практици и генетични лаборатории.
Ние сме убедени, че хранителните добавки, които предлагаме, ще ти помогнат да живееш по-здравословен, балансиран и щастлив живот. И ако по някаква причина това не е така, предлагаме пълно въстановяване на парите ти в 60-дневен срок от покупка (дори и да ни върнеш празни бутилки).
Искаме да се чувстваш уверен да опиташ L-methylfolate и другите ни добавки, без риск.
70 клинични проучвания за метилирането
MTHFR генетика и рискове
Frosst, P., et al. (1995). "A candidate genetic risk factor for vascular disease: a common mutation in methylenetetrahydrofolate reductase" Nature Genetics 10:111-113
Оригинално идентифициране на C677T полиморфизъм
Weisberg, I., et al. (1998). "A second genetic polymorphism in methylenetetrahydrofolate reductase (A1298C) associated with decreased enzyme activity" Molecular Genetics and Metabolism 64:169-172
Характеризиране на A1298C вариант
Wald, D.S., et al. (2002). "Homocysteine and cardiovascular disease: evidence on causality from a meta-analysis" BMJ 325:1202-1206
72 MTHFR studies, 16,849 cases
3 µmol/L ↓ homocysteine = 16% ↓ ischemic heart disease
Homocysteine Studies Collaboration (2002). "Homocysteine and risk of ischemic heart disease and stroke: a meta-analysis" JAMA 288:2015-2022
30 studies, 5,073 IHD events
25% ↓ homocysteine = 11% ↓ IHD risk, 19% ↓ stroke risk
Klerk, M., et al. (2002). "MTHFR 677C→T polymorphism and risk of coronary heart disease: a meta-analysis" JAMA 288:2023-2031
Meta-analysis: TT genotype = 16% increased CHD risk
Lewis, S.J., et al. (2005). "Meta-analysis of MTHFR 677C→T polymorphism and coronary heart disease: does totality of evidence support causal role for homocysteine and preventive potential of folate?" BMJ 331:1053
40 studies, 11,162 cases
Clarke, R., et al. (2010). "Effects of lowering homocysteine levels with B vitamins on cardiovascular disease, cancer, and cause-specific mortality" Archives of Internal Medicine 170:1622-1631
Meta-analysis of 8 RCTs, 37,485 participants
Lonn, E., et al. (2006). "Homocysteine lowering with folic acid and B vitamins in vascular disease" New England Journal of Medicine 354:1567-1577
HOPE-2 Trial: 5,522 patients
Wang, X., et al. (2007). "Efficacy of folic acid supplementation in stroke prevention: a meta-analysis" Lancet 369:1876-1882
China trial: 20,000+ participants, folic acid ↓ stroke by 21%
Zaccardi, F., et al. (2017). "Sauna bathing and incident hypertension: a prospective cohort study" American Journal of Hypertension 30:1120-1125
Л-метилфолат и депресия
Papakostas, G.I., et al. (2012). "L-methylfolate as adjunctive therapy for SSRI-resistant major depressive disorder: results of two randomized, double-blind, parallel-sequential trials" American Journal of Psychiatry 169:1267-1274
N=223, два RCTs
32.3% response rate vs 14.6% placebo
7.2x по-висока ремисия
Ginsberg, L.D., et al. (2011). "L-methylfolate plus SSRI or SNR improves depressive symptoms and function" Innovations in Clinical Neuroscience 8(1):19-28
Open-label extension, N=75
Shelton, R.C., et al. (2013). "Assessing outcomes for patients with major depressive disorder treated with L-methylfolate" Primary Care Companion CNS Disorders 15(5)
Real-world study: 67.9% response rate
Zajecka, J.M., et al. (2016). "Long-term efficacy, safety, and tolerability of L-methylfolate calcium 15 mg as adjunctive therapy with selective serotonin reuptake inhibitors" Journal of Clinical Psychiatry 77:654-660
Miller, A.L. (2008). "The methylation, neurotransmitter, and antioxidant connections between folate and depression" Alternative Medicine Review 13:216-226
Al Maruf, A., et al. (2022). "Efficacy of L-methylfolate in patients with major depressive disorder: A systematic review and meta-analysis" Pharmacopsychiatry 55:139-147
Meta-analysis of 9 studies, 6,707 patients
Relative risk 1.25 for response
Хомоцистеин и когнитивен спад
Seshadri, S., et al. (2002). "Plasma homocysteine as a risk factor for dementia and Alzheimer's disease" New England Journal of Medicine 346:476-483
Framingham study: Homocysteine >14 µmol/L = 2x risk of Alzheimer's
Smith, A.D., et al. (2010). "Homocysteine-lowering by B vitamins slows the rate of accelerated brain atrophy in mild cognitive impairment" PLoS ONE 5:e12244
Oxford study: B vitamins ↓ brain atrophy by 30%
Douaud, G., et al. (2013). "Preventing Alzheimer's disease-related gray matter atrophy by B-vitamin treatment" PNAS 110:9523-9528
B vitamins slow gray matter atrophy in high-risk MCI patients
Morris, M.S., et al. (2007). "Folate and vitamin B-12 status in relation to anemia, macrocytosis, and cognitive impairment in older Americans" American Journal of Clinical Nutrition 85:193-200
McCaddon, A., et al. (1998). "Homocysteine and cognitive decline in healthy elderly" Dementia and Geriatric Cognitive Disorders 9:316-326
MTHFR и психиатрични разтройства
Joffre, M., et al. (2012). "Genetic variation throughout the folate metabolic pathway influences negative symptom severity in schizophrenia" Schizophrenia Bulletin 38:1267-1274
Massachusetts General Hospital study
4 variants predict negative symptoms: MTHFR 677T, MTR 2756A, FOLH1 484C, COMT 675A
Liew, S.C., et al. (2018). "Methylenetetrahydrofolate reductase (MTHFR) C677T polymorphism: epidemiology, metabolism and the associated diseases" European Journal of Medical Genetics 61:759-769
Wu, Y.L., et al. (2013). "Association between MTHFR C677T polymorphism and depression: an updated meta-analysis" Journal of Affective Disorders 151:989-995
Gilbody, S., et al. (2007). "Methylenetetrahydrofolate reductase (MTHFR) genetic polymorphisms and psychiatric disorders: a HuGE review" American Journal of Epidemiology 165:1-13
V. DNA Methylation & Epigenetics
Esteller, M. (2007). "Cancer epigenomics: DNA methylomes and histone-modification maps" Nature Reviews Genetics 8:286-298
Comprehensive review of epigenetics in cancer
Choi, S.W., et al. (2009). "Folate and carcinogenesis: an integrated scheme" Journal of Nutrition 139:1897-1903
Folate's dual role in cancer prevention/promotion
Jaenisch, R., et al. (2003). "Epigenetic regulation of gene expression: how the genome integrates intrinsic and environmental signals" Nature Reviews Genetics 4:638-649
Crider, K.S., et al. (2012). "Folate and DNA methylation: a review of molecular mechanisms and the evidence for folate's role" Advances in Nutrition 3(1):21-38
Friso, S., et al. (2002). "A common mutation in the 5,10-methylenetetrahydrofolate reductase gene affects genomic DNA methylation through an interaction with folate status" PNAS 99:5606-5611
TT genotype has diminished DNA methylation vs CC
Бременност, репродуктивна система и неврални дефекти
VI. Reproduction, Pregnancy, Neural Tube Defects
van der Put, N.M., et al. (1998). "A second common mutation in the methylenetetrahydrofolate reductase gene: an additional risk factor for neural-tube defects?" American Journal of Human Genetics 62:1044-1051
Czeizel, A.E., et al. (1992). "Prevention of the first occurrence of neural-tube defects by periconceptional vitamin supplementation" New England Journal of Medicine 327:1832-1835
Landmark study: Folic acid ↓ NTDs by 70%
Wong, W.Y., et al. (2002). "Effects of folic acid and zinc sulfate on male factor subfertility: a double-blind, randomized, placebo-controlled trial" Fertility & Sterility 77:491-498
Folate + zinc increased sperm count by 74%
Nelen, W.L., et al. (2000). "Hyperhomocysteinemia and recurrent early pregnancy loss: a meta-analysis" Fertility & Sterility 74:1196-1199
High homocysteine = 2-3x miscarriage risk
Botto, L.D., et al. (2000). "5,10-Methylenetetrahydrofolate reductase gene variants and congenital anomalies: a HuGE review" American Journal of Epidemiology 151:862-877
Berry, R.J., et al. (1999). "Prevention of neural-tube defects with folic acid in China" New England Journal of Medicine 341:1485-1490
TMG (Бетаин)
Schwab, U., et al. (2002). "Betaine supplementation decreases plasma homocysteine concentrations but does not affect body weight, body composition, or resting energy expenditure in human subjects" Journal of Nutrition 132:1879-1883
TMG effectively lowers homocysteine
Olthof, M.R., et al. (2005). "Low dose betaine supplementation leads to immediate and long term lowering of plasma homocysteine in healthy men and women" British Journal of Nutrition 93:593-600
Dose-response relationship established
McGregor, D.O., et al. (2002). "Betaine supplementation decreases post-methionine hyperhomocysteinemia in chronic renal failure" Kidney International 61:1040-1046
Steenge, G.R., et al. (2003). "Betaine supplementation lowers plasma homocysteine in healthy men and women" Journal of Nutrition 133:1291-1295
Метилирането и сърдечното здраве
Bønaa, K.H., et al. (2006). "Homocysteine lowering and cardiovascular events after acute myocardial infarction" New England Journal of Medicine 354:1578-1588
NORVIT trial
Toole, J.F., et al. (2004). "Lowering homocysteine in patients with ischemic stroke to prevent recurrent stroke, myocardial infarction, and death: the Vitamin Intervention for Stroke Prevention (VISP) randomized controlled trial" JAMA 291:565-575
Bazzano, L.A., et al. (2006). "Effect of folic acid supplementation on risk of cardiovascular diseases: a meta-analysis of randomized controlled trials" JAMA 296:2720-2726
Verhaar, M.C., et al. (1998). "5-methyltetrahydrofolate, the active form of folic acid, restores endothelial function in familial hypercholesterolemia" Circulation 97:237-241
Метилирането и възпаление
Jeffries, M.A., et al. (2011). "Genome-wide DNA methylation patterns in CD4+ T cells from patients with systemic lupus erythematosus" Clinical Immunology 140:242-251
Niculescu, M.D., et al. (2006). "Nutritional genomics: folate and DNA methylation" Annual Review of Nutrition 26:131-155
Yi, P., et al. (2000). "Increase in plasma homocysteine associated with parallel increases in plasma S-adenosylhomocysteine and lymphocyte DNA hypomethylation" Journal of Biological Chemistry 275:29318-29323
Метаболизма на фолат и биохимия
Stover, P.J. (2009). "One-carbon metabolism-genome interactions in folate-associated pathologies" Journal of Nutrition 139:2402-2405
Shane, B., et al. (1989). "Folate chemistry and metabolism" Clinical Nutrition 1:1-22
Schalinske, K.L., et al. (2003). "Folate supplementation overrides the metabolic defect associated with the methylenetetrahydrofolate reductase C677T polymorphism" American Journal of Clinical Nutrition 77:1304-1309
5-MTHF срещу фолиева киселина - биоусвояемост
Venn, B.J., et al. (2002). "Comparison of the effect of low-dose supplementation with L-5-methyltetrahydrofolate or folic acid on plasma homocysteine" American Journal of Clinical Nutrition 77:658-662
L-5-MTHF more effective than folic acid
Lamers, Y., et al. (2006). "Supplementation with [6S]-5-methyltetrahydrofolate or folic acid equally reduces plasma total homocysteine concentrations in healthy women" American Journal of Clinical Nutrition 84:156-161
Prinz-Langenohl, R., et al. (2009). "6S-5-methyltetrahydrofolate increases plasma folate more effectively than folic acid in women with the homozygous or wild-type 677C→T polymorphism of methylenetetrahydrofolate reductase" British Journal of Pharmacology 158:2014-2021
Pietrzik, K., et al. (2010). "Folic acid and L-5-methyltetrahydrofolate: comparison of clinical pharmacokinetics and pharmacodynamics" Clinical Pharmacokinetics 49:535-548
Houghton, L.A., et al. (2006). "Unmetabolized folic acid and total folate concentrations in breast milk are unaffected by low-dose folate supplements" American Journal of Clinical Nutrition 83:664-670
MTHFR дефицит и лечение
Crushell, E., et al. (2012). "Homocystinuria due to severe methylenetetrahydrofolate reductase deficiency: clinical management and mutation analysis" Clinical Genetics 81:520-526
Strauss, K.A., et al. (2007). "MTHFR deficiency as a cause of severe homocystinuria and neonatal cerebral hemorrhage" Journal of Pediatrics 151:334-337
Huemer, M., et al. (2016). "Treatment with 5-methyltetrahydrofolate (mefolinate), but not folic acid or folinic acid, leads to measurable 5-methyltetrahydrofolate in cerebrospinal fluid in methylenetetrahydrofolate reductase deficiency" JIMD Reports 29:81-86
Mayo Clinic case series
MTHFR полимни орфизми
Wilcken, B., et al. (2003). "Geographical and ethnic variation of the 677C>T allele of 5,10 methylenetetrahydrofolate reductase (MTHFR): findings from over 7000 newborns from 16 areas world wide" Journal of Medical Genetics 40:619-625
Global prevalence data
Tsang, B.L., et al. (2015). "Assessing the association between the methylenetetrahydrofolate reductase (MTHFR) 677C>T polymorphism and blood folate concentrations: a systematic review and meta-analysis of trials and observational studies" American Journal of Clinical Nutrition 101(6):1286-1294
Crider, K.S., et al. (2011). "MTHFR 677C→T genotype is associated with folate and homocysteine concentrations in a large, population-based, double-blind trial of folic acid supplementation" American Journal of Clinical Nutrition 93(6):1365-1372
Метилфолат, митохондрии и клетъчна енергия
Suormala, T., et al. (2004). "The cblE gene confers susceptibility to combined deficiency of methionine synthase and methylmalonic aciduria: homocystinuria, methylenetetrahydrofolate reductase and cobalamin C disease" Molecular Genetics and Metabolism 83:208-213
Loehrer, F.M., et al. (2001). "Impaired DNA biosynthesis in mitochondria from patients with impaired deoxycytidine kinase activity" Circulation 104:2569-2575
Глутатион и детоксикация
XV. Glutathione & Detoxification
Lu, S.C. (2009). "Regulation of glutathione synthesis" Molecular Aspects of Medicine 30:42-59
James, S.J., et al. (2004). "Metabolic biomarkers of increased oxidative stress and impaired methylation capacity in children with autism" American Journal of Clinical Nutrition 80:1611-1617
Miller, A.L. (2008). "The methylation, neurotransmitter, and antioxidant connections between folate and depression" Alternative Medicine Review 13:216-226
Подробни прегледи и насоки
Hannekkela, M.L., et al. (2001). "Benefits and risks of sauna bathing" The American Journal of Medicine 114:118-126
Crinnion, W.J. (2011). "Sauna as a valuable clinical tool for cardiovascular, autoimmune, toxicant- induced and other chronic health problems" Alternative Medicine Review 16:215-225
Den Heijer, M., et al. (2005). "Hyperhomocysteinemia as a risk factor for deep-vein thrombosis" New England Journal of Medicine 352:2034-2041
Leclerc, D., et al. (2000). "Molecular biology of methylenetetrahydrofolate reductase (MTHFR) and overview of mutations/polymorphisms" Madame Curie Bioscience Database
